Тіло масою 2 кг, рухаючись по інерції до повної зупинки, за 5 с пройшло шлях 1,25 м вздовж похилої площини, що утворює кут 35° з горизонтом. Знайдіть роботу сил тертя і початкову швидкість тіла.
Учитывая, что начальная скорость вертолете ноль, найдем высоту h, на которую он поднялся за время t по формуле
h = a/2 (1), здесь a - ускорение с которым поднимается вертолет.
Подставляя данные из условия в формулу (1) получим. h = 4*/2 = 200 метров. Скорость V с которой движется вертолет составит V = at = 4*10 = 40 м/сек.
Теперь для предмета, упавшего из вертолета: его начальная скорость будет равна скорости вертолета, т.е. 40 м/сек и вектор скорости направлен вверх. На предмет будет действовать сила тяжести, придающая ему ускорение g = 9,8 м/сек, направленная вниз. Таким образом, за время t = V/g (2) скорость предмета станет равной нулю. Подставляя в (2) наши данные получим, t = 40/9,8 = 4,08 сек. За это время предмет дополнительно поднимется на высоту
h1 = Vt - g/2 = 40*4,08 - 10*16,64/2 = 81,63 м.
h2 = h+h1 = 200 + 81,63 = 281,63
Для тела, падающего с высоты h2 без начальной скорости имеем
h2 = g/2
Отсюда получаем t = = = 7,58 сек
К этому времени надо добавить 4,08 сек, что предмет летел вверх. Получаем
Чтобы рассчитать массу соли, образующейся в результате реакции между гидроксидом натрия и серной кислотой, необходимо знать сбалансированное химическое уравнение реакции. Сбалансированное уравнение: NaOH + H2SO4 → Na2SO4 + 2H2O. Стехиометрическое отношение NaOH к Na2SO4 составляет 1:1, что означает, что на каждый 1 моль используемого NaOH получается 1 моль Na2SO4. Молярная масса Na2SO4 142,04 г/моль. Поэтому для расчета массы образовавшегося Na2SO4 необходимо знать количество молей NaOH, использованных в реакции. Получив это значение, вы можете умножить его на молярную массу Na2SO4, чтобы получить массу произведенного Na2SO4.
Чтобы найти объем двуокиси серы, образующейся при обжиге пирита с примесями, нужно знать сбалансированное химическое уравнение реакции. Сбалансированное уравнение: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2. Это означает, что на каждые 4 моля используемого FeS2 производится 8 молей SO2. Молярная масса SO2 составляет 64,06 г/моль. Чтобы рассчитать объем произведенного SO2, вам необходимо знать количество молей FeS2, использованных в реакции, и условия реакции (например, температуру и давление). Получив эту информацию, вы можете использовать закон идеального газа для расчета объема произведенного SO2. В качестве альтернативы, если вы знаете массу FeS2, использованного в реакции, вы можете использовать стехиометрию для расчета количества молей FeS2, а затем количество молей образовавшегося SO2.
t = 11,7 сек. (приближенно)
Объяснение:
Учитывая, что начальная скорость вертолете ноль, найдем высоту h, на которую он поднялся за время t по формуле
h = a /2 (1), здесь a - ускорение с которым поднимается вертолет.
/2 (1), здесь a - ускорение с которым поднимается вертолет.
Подставляя данные из условия в формулу (1) получим. h = 4* /2 = 200 метров. Скорость V с которой движется вертолет составит V = at = 4*10 = 40 м/сек.
/2 = 200 метров. Скорость V с которой движется вертолет составит V = at = 4*10 = 40 м/сек.
Теперь для предмета, упавшего из вертолета: его начальная скорость будет равна скорости вертолета, т.е. 40 м/сек и вектор скорости направлен вверх. На предмет будет действовать сила тяжести, придающая ему ускорение g = 9,8 м/сек, направленная вниз. Таким образом, за время t = V/g (2) скорость предмета станет равной нулю. Подставляя в (2) наши данные получим, t = 40/9,8 = 4,08 сек. За это время предмет дополнительно поднимется на высоту
h1 = Vt - g /2 = 40*4,08 - 10*16,64/2 = 81,63 м.
/2 = 40*4,08 - 10*16,64/2 = 81,63 м.
h2 = h+h1 = 200 + 81,63 = 281,63
Для тела, падающего с высоты h2 без начальной скорости имеем
h2 = g /2
/2
Отсюда получаем t = =
= 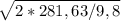 = 7,58 сек
= 7,58 сек
К этому времени надо добавить 4,08 сек, что предмет летел вверх. Получаем
t = 7,58 + 4,08 = 11,66 сек. = 11,7 сек.
Чтобы рассчитать массу соли, образующейся в результате реакции между гидроксидом натрия и серной кислотой, необходимо знать сбалансированное химическое уравнение реакции. Сбалансированное уравнение: NaOH + H2SO4 → Na2SO4 + 2H2O. Стехиометрическое отношение NaOH к Na2SO4 составляет 1:1, что означает, что на каждый 1 моль используемого NaOH получается 1 моль Na2SO4. Молярная масса Na2SO4 142,04 г/моль. Поэтому для расчета массы образовавшегося Na2SO4 необходимо знать количество молей NaOH, использованных в реакции. Получив это значение, вы можете умножить его на молярную массу Na2SO4, чтобы получить массу произведенного Na2SO4.
Чтобы найти объем двуокиси серы, образующейся при обжиге пирита с примесями, нужно знать сбалансированное химическое уравнение реакции. Сбалансированное уравнение: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2. Это означает, что на каждые 4 моля используемого FeS2 производится 8 молей SO2. Молярная масса SO2 составляет 64,06 г/моль. Чтобы рассчитать объем произведенного SO2, вам необходимо знать количество молей FeS2, использованных в реакции, и условия реакции (например, температуру и давление). Получив эту информацию, вы можете использовать закон идеального газа для расчета объема произведенного SO2. В качестве альтернативы, если вы знаете массу FeS2, использованного в реакции, вы можете использовать стехиометрию для расчета количества молей FeS2, а затем количество молей образовавшегося SO2.