По уравнению реакции, мы видим, чтобы полностью растворитьцинк в кислоте, нам понадобится кислота количеством вещества в два раза больше, т.е 0,4 моль
Рассчитаем количество вещества кислоты, для этого узнаем ее массу:
m = p*V = 200мл*1,1г/мл = 220грамм
n = m/M = 220г/36,5г/моль ~ 6моль
Ну что тут сказать...Тут кислота не то что растворит цинк, она еще и останется, т.е. мы можем смело заяавить, что такой объем кислоты хватит для полного растворения 13 грамм цинка
1. a) CaO,
в)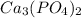
б) HCl
г)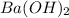
д)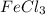
2. Азотная кислота, оксид алюминия (3), гидроксид кальция, сульфат магния, ортофосфорная кислота
3.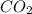 , MgO,
, MgO, 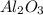 ,
, 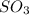 ,
, 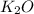
4. В первом +3(промежуточная), во втором -3(низшая), в третьем +5(высшая), в четвертом +2(промежуточная).
5. Решим простую математическую задачу: 200л(полный объем воздуха) * 21%(о,21) = 42 л кислорода
6. Найдём массу1 сахара = о,2 * 80 = 16 кг
найдем массу сахара2 = 16 + 15 = 31 кг
найдем массу раствора2 = 80 + 15 = 95 кг
И новая массовая доля равна: 31/95 * 100% (масса вещества/массу раствора) = 32,63 % или 33%
Запишем уравнение реакции:
Zn + 2HCl = ZnCl2 + h2
Рассчитаем количество вещества цинка:
n = m/M = 13г/65г/моль = 0,2 моль
По уравнению реакции, мы видим, чтобы полностью растворитьцинк в кислоте, нам понадобится кислота количеством вещества в два раза больше, т.е 0,4 моль
Рассчитаем количество вещества кислоты, для этого узнаем ее массу:
m = p*V = 200мл*1,1г/мл = 220грамм
n = m/M = 220г/36,5г/моль ~ 6моль
Ну что тут сказать...Тут кислота не то что растворит цинк, она еще и останется, т.е. мы можем смело заяавить, что такой объем кислоты хватит для полного растворения 13 грамм цинка