9класс , 50 !
контрольная работа №1 по теме "металлы"
часть а
1) сколько электронов содержат на внешнем энергическом уровне атомы щелочных металлов?
1) один 2) два 3) три 4) четыре
2) в реакциях атомы натрия проявляют:
1) окислительные свойства 2) кислотные св-ва 3) восстановительные св-ва
4) основные св-ва
3) взаимодействие кальция с водой относиться к реакциям:
1) разложения 2) соединения 3) замещения 4) обмена
4) наиболее энергично реагирует с водой:
a) барий б) кальций в) магний г) стронций
5) с соляной кислотой не взаимодействует:
а) алюминий б) магний в) серебро г) цинк
6) гидроксид алюминия взаимодействует с веществом, формула которого:
а) baso₄ б) naoh в) kcl (растворённый) г) nano₃ (растворённый)
7) ряд в котором все вещества реагируют с железом:
а) hcl, co₂, co б) cl₂, cucl₂, hcl в) h₂, o₂, cao г) sio₂, hcl, s
8) элементом x в схеме превращений x---> x₂0---> xoh является:
а) барий б) литий в) серебро г) углерод
часть b
1. что такое коррозия металлов? какие виды коррозии вам известны? какие факторы замедлению, какие - усилению коррозии металлов?
2. примеры металлов: а) тугоплавких и легкоплавких;
серебристо-серых и имеющих цвет.
3. в каком виде встречаются металлы в природе? почему?
часть с ( 5 )
i. составьте электронную схему атома для элемента с порядковым номером 19,
c которой дайте ответы на следующие вопросы:
a) положение в псхэ (период, группа, подгруппа).
б) количество электронов на внешнем энергетическом уровне,
b) восстановительная степень окисления, формула высшего оксида, его характер
и название
г. формула гидроксида, его характер и название.
2. составить уравнения реакций и показать их как окислительно - восстановительные.
a) ва + h₂0 б) al + v₂o₅
3. расставить коэффициенты в схеме реакции методом электронного :
cu + hno₃ - cu(no₃)₂, + no + h₂o
4. составить уравнения реакций и показать их как реакции ионного обмена:
a) cu(oh), + hno,
б) nacl + agno, --
5. осуществить следующие превращения:
fe - fecl fe(oh) - fe - feso,
б) al + v2o, -
, сделайте хотябы часть, буду
ответ: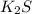
Объяснение к ответу: Начнём с условия. В условии сказано, что в формуле на первом месте нужно записать химический знак элемента. Химический элемент из самого условия это Калий, его знак это K. Ставим теперь этот химический знак, далее по условию "на втором — химический знак серы." Это значит, что после К мы пишем химический знак серы S. Мы знаем, что индекс - это число, показывающее количество атомов данного химического элемента в молекуле вещества. Индекс у нас равен 2, так как в соединении калия с серой: сера имеет валентность равную II, а калий I. Значит у Калия индекс будет 2, а у Серы 1.
На заметку: Соединения с серой называются сульфидами и сера в таких соединениях имеет степень окисления -2 или валентность равную двум.
Объяснение:
2) 4 г Х г
2Ca + O2 = 2CaO
n=2 моль n=2 моль
М = 40 г/моль М = 56 г/моль
m = 80 г m=112 г
4 г Са - Х г СаО
80 г Са - 112 г СаО
m(CaO) = 4 * 112 / 80 = 5,6 г
3) Х л 20 г
2Mg + O2 = 2MgO
n=1 моль n=2 моль
Vm=22,4 л/моль М = 40 г/моль
V = 22,4 л m=80 г
Х л О2 - 20 г MgO
22,4 л О2 - 80 г MgO
V(O2) = 22,4 * 20 / 80 = 5,6 л
4 моль Х г
4) CuO + H2SO4 = CuSO4 + H2O
n=1 моль n=1 моль
М = 160 г/моль
m=160 г
4 моль CuO - Х г CuSO4
1 моль CuO - 160 г CuSO4
m(CuSO4) = 4 * 160 / 1 = 640 г