3. Во-первых, мы сразу видим что это химическая формула соли угольной кислоты и кальция. По другому, мы её ещё называем - карбонат кальция. Видим качественный(состоит из трех химических элементов: Ca, C, O) и количественный - в состав входит 1 атом кальция(Ca), 1 атом углерода(C) и 3 атома кислорода(O), составы. Молярную массу, равную 100 г/моль: г/моль. Массовую долю всех химических элементов в составе соли:
Соотношение массы хим.элементов: 40:12:48
4. Простые вещества - вещества, состоящие из одного хим.элемента.
Кислотные свойства в одном растворе проявляют галогеноводороды и некоторые халькогеноводороды (H2S, H2Se).
3. сначала нужно воспользоваться хлоридом бария (BaCl2). В пробирке с серной кислотой выпадет белый осадок. В оставшиеся две пробирки налить нитрат серебра (AgNO3). В пробирке с соляной кислотой выпадет белый осадок. Оставшаяся пробирка - с гидроксидом натрия.
4. P2O5 + 3H2O = 2H3PO4
P2O5 + 6NaOH = 2Na3PO4 + 3H2O
P2O5 + 3CaO = Ca3(PO4)2
фосфорная кислота реагирует с металлами до водорода в электрохимическом ряду напряжений металлов:
3. Во-первых, мы сразу видим что это химическая формула соли угольной кислоты и кальция. По другому, мы её ещё называем - карбонат кальция. Видим качественный(состоит из трех химических элементов: Ca, C, O) и количественный - в состав входит 1 атом кальция(Ca), 1 атом углерода(C) и 3 атома кислорода(O), составы. Молярную массу, равную 100 г/моль: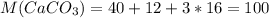 г/моль. Массовую долю всех химических элементов в составе соли:
г/моль. Массовую долю всех химических элементов в составе соли: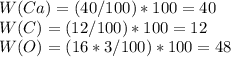
Соотношение массы хим.элементов: 40:12:48
4. Простые вещества - вещества, состоящие из одного хим.элемента.
Подходят: Б) озон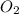 , В) железо
, В) железо 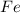 ;
;
5. О простом веществе: Б, Г;
О хим.элементе: А, В, Д
Непосредсвенный синтез из водорода и хлора:
H2 + Cl2 = 2HCl
Вытеснение сильной кислотой из соли:
2NaCl + H2SO4 = Na2SO4 + 2HCl
2. Твердые: ортофосфорная кислота, борная кислота.
Жидкие: серная кислота, азотная кислота.
Кислотные свойства в одном растворе проявляют галогеноводороды и некоторые халькогеноводороды (H2S, H2Se).
3. сначала нужно воспользоваться хлоридом бария (BaCl2). В пробирке с серной кислотой выпадет белый осадок. В оставшиеся две пробирки налить нитрат серебра (AgNO3). В пробирке с соляной кислотой выпадет белый осадок. Оставшаяся пробирка - с гидроксидом натрия.
4. P2O5 + 3H2O = 2H3PO4
P2O5 + 6NaOH = 2Na3PO4 + 3H2O
P2O5 + 3CaO = Ca3(PO4)2
фосфорная кислота реагирует с металлами до водорода в электрохимическом ряду напряжений металлов:
3Zn + 2H3PO4 = Zn3(PO4)2 + 3H2
c основными и амфотерными оксидами:
33CaO + 2H3PO4 = Ca3(PO4)2 + 3H2O
с основаниями:
3NaOH + H3PO4 = Na3PO4 + 3H2O
c солями более слабых кислот:
3Na2CO3 + 2H3PO4 = 2Na3PO4 + 3H2O + 3CO2
c аммиаком:
2NH3 + H3PO4 = (NH4)2HPO4