1.кислородсодержащие органические соединения, в которых атом Водорода, замещен на одну карбоксильную группу, называются предельные одноосновные кислоты.
2.муравьиную кислоту можно получить действием на ее соли более сильными кислотами,например,серной.А ее соль можно получить,пропуская угарный газ через нагретую щелочь
3.Фенол обладает следующими физическими свойствами:бесцветное кристаллическое вещество со специфическим запахом,температурой плавления 42,3 градуса по Цельсию,температурой кипения 181,1 градуса,довольно трудно растворим в воде,на воздухе окисляется(краснеет) и кристаллы его расплываются.
4.область применения формальдегида:в производстве пластмасс,в кожевенном деле для дубления кожи,медицине и санитарии - для дезинфекции,40%-водный раствор называют формалином и применяют в семеноводстве для протравливания зерна от грибковых заболеваний
№2 составить формулу: 3-этилгептаналь:
7 6 5 4 3 2 1
| |
№3 закончить уравнение следующих реакций, укажите условия протекания, назовите вещества:
С2Н2--->СН3СОН--->С2Н5ОН--->НСООС2Н5 1)(в присутствии раствора сульфата ртути)- реакция Кучерова
2)(в присутствии никеля)
3)(при незначительном нагревании в присутствии концентрированной серной кислоты)
1) n = m/M; где m — масса вещества ( даётся по условию ), M — молекулярная масса из таблицы
2) n = V/Vm; где V — объём ( даётся по условию ), Vm — молярный объём для всех газов, константа, равняется 22.4 л/моль
3) n = N/Na; где N — количество частиц, Na — число Авогадро, константа, равняется 6.02*10²³ частиц.
a) Нам дано 5 моль Н2. 5 моль — это количество вещества, обозначаем как n(H2) = 5 моль. Нам нужно узнать массу (m) и количество частиц (N).
Нам дано количество этого вещества ( n = 5 моль ), нужно узнать массу (m) и количество частиц (N).
Берём формулу, где есть масса, т.е. первая: n = m/M
Нам дано n и мы можем рассчитать M из таблицы Менделеева: M(H2) = M(H) + M(H) = 1 + 1 = 2 г/моль
Подставляем известные нам величины в формулу:
5 = m/2 ==> m = 5*2 = 10 грамм.
Масса найдена. Теперь переходим к формуле с количеством частиц: n = N/Na.
n нам всё ещё дано, Na — константа, 6.02*10²³. Для того, чтобы найти количество частиц, снова просто подставляем всё это в формулу:
5 = N/6.02*10²³ ==> N = 5*6.02*10²³ = 31*10²³ частиц.
Количество частиц и масса найдены, задание выполнено.
b) Дано:
n(CO2) = 7 моль
Найти: m и N.
Тот же принцип:
n = m/M
m = n*M = 7*M(CO2) = 7*(12+16+16) = 7*44 = 308 грамм
n = N/Na
N = n*Na = 7*6.02*10²³ = 42.14*10²³ частиц.
c) Дано:
n(H3PO4) = 0.1 моль
Найти: m и N.
n = m/M
m = n*M = 0.1*M(H3PO4) = 0.1*(3+31+16*4) = 0.1*98 = 9.8 грамм
n = N/Na
N = n*Na = 0.1 * 6.02 * 10²³ = 0.602*10²³ частиц.
Объяснение:
1.кислородсодержащие органические соединения, в которых атом Водорода, замещен на одну карбоксильную группу, называются предельные одноосновные кислоты.
2.муравьиную кислоту можно получить действием на ее соли более сильными кислотами,например,серной.А ее соль можно получить,пропуская угарный газ через нагретую щелочь
3.Фенол обладает следующими физическими свойствами:бесцветное кристаллическое вещество со специфическим запахом,температурой плавления 42,3 градуса по Цельсию,температурой кипения 181,1 градуса,довольно трудно растворим в воде,на воздухе окисляется(краснеет) и кристаллы его расплываются.
4.область применения формальдегида:в производстве пластмасс,в кожевенном деле для дубления кожи,медицине и санитарии - для дезинфекции,40%-водный раствор называют формалином и применяют в семеноводстве для протравливания зерна от грибковых заболеваний
№2 составить формулу: 3-этилгептаналь:
7 6 5 4 3 2 1
| |
№3 закончить уравнение следующих реакций, укажите условия протекания, назовите вещества:
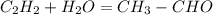 (в присутствии раствора сульфата ртути)- реакция Кучерова
(в присутствии раствора сульфата ртути)- реакция Кучерова
С2Н2--->СН3СОН--->С2Н5ОН--->НСООС2Н5
1)
2)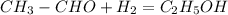 (в присутствии никеля)
(в присутствии никеля)
3)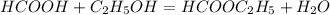 (при незначительном нагревании в присутствии концентрированной серной кислоты)
(при незначительном нагревании в присутствии концентрированной серной кислоты)