Запишем уравнение реакции и расставим степень окисления у тех элементов, которые меняют её в ходе реакции:
ᅠᅠ
Проводим электронный баланс:
ᅠᅠ| 2 | 3 | окисление
ᅠᅠ | 3 | 2 | восстановление
ᅠᅠHNO₃ (N⁺⁵) - окислитель, Cu - восстановитель.
Полученные коэффициенты ставим в уравнение: 2 перед NO, 3 перед Cu и Cu(NO₃)₂:
Уравниваем оставшиеся атомы:
Сверяем количество атомов в правой и левой части, чтобы удостовериться, что мы уравняли верно:
Запишем уравнение реакции и расставим степень окисления у тех элементов, которые меняют её в ходе реакции:
ᅠᅠ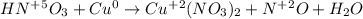
Проводим электронный баланс:
ᅠᅠ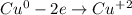
 | 2 | 3 | окисление
| 2 | 3 | окисление
ᅠᅠ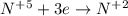 | 3 | 2 | восстановление
| 3 | 2 | восстановление
ᅠᅠHNO₃ (N⁺⁵) - окислитель, Cu - восстановитель.
Полученные коэффициенты ставим в уравнение: 2 перед NO, 3 перед Cu и Cu(NO₃)₂:
ᅠᅠ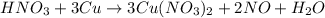
Уравниваем оставшиеся атомы:
ᅠᅠ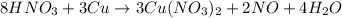
Сверяем количество атомов в правой и левой части, чтобы удостовериться, что мы уравняли верно:
ᅠᅠ![\left[\begin{array}{ccc}&\bold{Left}&\bold{Right}\\\bold{H}&8&8\\\bold{N}&8&8\\\bold{O}&24&24\\\bold{Cu}&3&3\end{array}\right]](/tpl/images/1478/3265/c4c6b.png)