Контрольная работа по теме: «Азот и фосфор» 9класс
Вариант № 1
Задание № 1
Определите тип химической связи в каждом из предложенных соединений. Расставьте над каждым элементом, входящим в состав соединения степень окисления. Назовите каждое соединение.
HNO3, Li3N, NO2, N2, NH3, NH4NO3, NaNO2, Ca3P2, NaH2PO4, PH3
Задание № 2
Напишите возможные с точки зрения обратимости уравнения реакции:
Нитрат цинка и серная кислота 3)азотная кислота и хлорид серебра
Карбонат калия и азотная кислота 4) нитрат натрия и сульфид бария
Во всех возможных реакциях напишите молекулярное, полное ионное и сокращённое ионное уравнения.
Задание № 3
Рассчитайте массовую долю азота в фосфате аммония.
Задание № 4
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции:
NH3 + CuO Cu + N2 + H2O
P + HNO3 + H2O H3PO4 + NO
Укажите окислитель и восстановитель.
Задание № 5
Используя сокращенное ионное уравнения составьте молекулярное и полное ионное уравнение:
3Ca2+ + 2PO43- Ca3(PO4)2
Задание № 6
Закончите уравнение реакций, расставьте коэффициенты, назовите полученные продукты реакции.
HNO3 (конц) + Mg
N2O5 + Mg(OH)2
NH3 + H2SO4
Ca3P2 + HCl
1. Насыщенные углеводороды: 4) называют алканами (алканы являются насыщенными углеводородами, так как в них отсутствуют кратные связи, и все свободные связи углерода образуют связь с атомами водорода)
2. Укажите химическую формулу радикала этила: 3) C₂H₅ (или в структурном виде -CH₂-CH₃)
3. Определите общую формулу алканов: 3)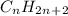
4. Какой тип гибридизации орбиталей атомов углерода реализуется в молекулах алканов?: 3) sp³ (углерод в молекулах алканов находится в sp³-гибридизации: гибридизируются все 4 орбитали - одна s-орбиталь и три p-орбиталей)
5. К алканам относится: 2) CH₄ (CH₄ - метан, углеводород классов алканов, так же соответствует их общей формуле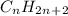 )
)
6) Какой тип изомерии характерен для алканов: 1) структурная изомерия
7. Назовите следующие соединения по заместительной номенклатуре.
1) 2-метилпентан:
ᅠᅠ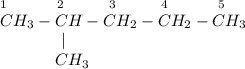
2) 2,3-диметилбутан:
ᅠᅠ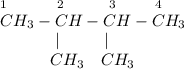
3) 2,3-диметилгексан:
ᅠᅠ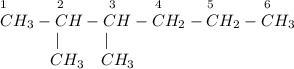
4) 2,5-диметил-3-этилгексан:
ᅠᅠ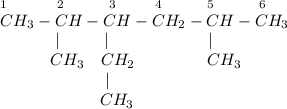
5) 2,3-диметил-4-пропил-6-этилоктан:
ᅠᅠ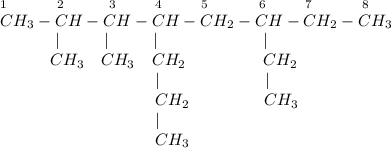
6) 2-хлорбутан:
ᅠᅠ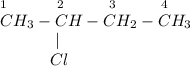
7) 2-нитробутан:
ᅠᅠ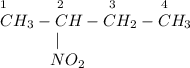
8) 2,5-диметил-3,4-диэтилгексан:
ᅠᅠ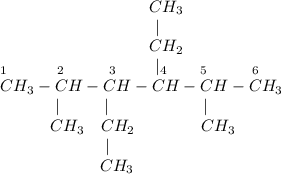
9) 2,2,6,8,8-пентаметил-3,3-диэтилнонан:
ᅠᅠ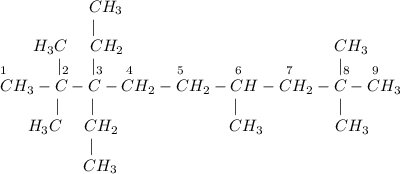
m(KMnO₄)=100г.
Vm(O₂) =22,4л./моль
V(O₂) -?
1. Запишем уравнение реакции разложения перманганата калия:
2KMnO₄ = K₂MnO₄ +MnO₂ + O₂
2. Определяем молярную массу перманганата калия:
M(KMnO₄)= 39+54,9+16х4=157г./моль
3. Определяем количество вещества n в 100г. перманганата калия по формуле:
n=m÷M n(KMnO₄) = 100г.÷157,5=0,63моль
4. Анализируем уравнение реакции: при разложении 2 моль перманганата калия выделяется 1 моль кислорода, значит при разложении 0,63моль перманганата калия выделится в два раза меньше кислорода:
0,63÷2=0,31моль кислорода.
5. Определяем объем кислорода количеством вещества 0,31моль по формуле: V=n x Vm V(O₂) = 0,31моль х 22,4л./моль=7,05л. O₂
6. ответ : при разложении 100г. перманганата калия выделится кислород объемом 7,05л