Изменение температуры влияет на равновесие, поскольку ΔG=ΔH-TΔS, а K - константа равновесия = exp(-ΔG/R/T)=exp((TΔS-ΔH)/R/T)=exp(ΔS/R-ΔH/R/T) также K равна так как сверху и снизу давление во второй степени суммарно, то K= то есть при изменении концентрации иода равновесие сместится, а при изменении давления - нет, таким образом, ответ 3 - увеличение давления
увеличение давления
Объяснение:
Изменение температуры влияет на равновесие, поскольку ΔG=ΔH-TΔS, а K - константа равновесия = exp(-ΔG/R/T)=exp((TΔS-ΔH)/R/T)=exp(ΔS/R-ΔH/R/T) также K равна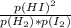 так как сверху и снизу давление во второй степени суммарно, то K=
так как сверху и снизу давление во второй степени суммарно, то K= 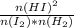 то есть при изменении концентрации иода равновесие сместится, а при изменении давления - нет, таким образом, ответ 3 - увеличение давления
то есть при изменении концентрации иода равновесие сместится, а при изменении давления - нет, таким образом, ответ 3 - увеличение давления