Неметалл, схема строения атома которого 2ē, 8ē, 6ē, образует высший оксид ЭО3. Задача. Определите массу (г) соли, которая образуется при взаимодействии этого высшего оксида массой 160 г с избытком гидроксида калия.
решить задачу по химии за 8 класс,
Відповідь:
Дано: w(C)=40%, w(H)=6.66%
I. Нехай у нас буде 100 грам невідомої органічної речовини. Отже, у нас буде m(C)=40 g , m(H)=6.66 g
w(O)=m(O)=100-40-6.66=53,34 g
II. Складемо співвідношення речовин, як n(C):n(H):n(O)
Тобто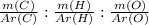
3.33 : 6.66 : 3.33
Беремо найменше число за одиницю.
1 : 6.66/3.33 : 1
1 : 2: 1
III. Запишемо формули // Виконаємо обчислення :
Отже найпростіша формула речовини є CH₂O
Ця формула існує, тому вона є істинною. Має назву формальдегід, який можна придбати в аптеці або ж у відділлі косметики, бо формальдегід, хоч і токсичний, але у малій концетрації прискорює регенерацію
*Поставте найкраще, будь ласка :)
Уравнение реакции образования сульфида:
Fe + S = FeS
M(Fe) = 56 г./моль
Количество вещества n( Fe) = 14÷56 = 0,25 моль
M = 32 г./моль
Количество вещества n(S) = 4,8÷32 = 0,15 моль.
Вывод: Железо находится в избытке равном: 0,25-0,15 = 0,1 моль.
В реакции образуется соответственно 0,1 моль сульфида цинка FeS.
2) Уравнение реакций взаимодействия железа и сульфида железа с соляной кислотой:
а) Fe + 2HCl = FeCl2 + H₂
б) FeS + 2HCl = ZnCl2 + H₂S;
в) соответственно:
1) из 0,1 моль Fe получится 0,1 моль H₂
V(H₂)= 0,1мольх22,4л./моль=2,24л.
2) из 0,15 моль FeS — соответственно 0,15 моль H₂S V(H₂S)=0,15мольх22,4л.моль=3,36л.
3. ответ: при сплавлении 14г. железа и 4,8г. серы, обработанного в дальнейшем соляной кислотой, выделился водород 2,24л. и сероводород 3,36л.
Объяснение: