1)2P+3Ca=Ca₃PO₄ Ca₃PO₄+6H₂O=3Ca(OH)₂+2PH₃ 2PH₃+4O₂=P₂O₅+3H₂O P₂O₅+H₂O=2HPO₃ HPO₃+H₂O=H₃PO₄ 2)3NaOH+H₃PO₄=Na₃PO₄+3H₂O 3Na(+)+3OH(-)+3H(+)+PO₄(3-)=3Na(+)+PO₄(3-)+3H₂O 3OH(-)+3H(+)=3H₂O,сокращаем на 3,получается: OH(-)+H(+)=H₂O 2FeCl₃+3Ca(OH)₂=2Fe(OH)₃+3CaCl₂ 2Fe(3+)+6Cl(-)+3Ca(2+)+6OH(-)=2Fe(OH)₃+3Ca(2+)+6Cl(-) 2Fe(3+)+6OH(-)=2Fe(OH)3,сокращаем на 2,получается: Fe(3+)+3OH(-)=Fe(OH)3 3)NaNO3(не подвергается гидролизу,потому что образована сильной кислотой и основанием) FeCl₃-основана слабым основанием и сильной кислотой,гидролиз идет по катиону 1 ступень FeCl3+HOH⇔FeOHCl2+HCl Fe(3+)+3Cl(-)+H2O⇔FeOH(2+)+2Cl(-)+H(+)+Cl(-) Fe(3+)+H2O⇔FeOH(2+)+H(+) 2 ступень FeOHCl2+H2O⇔Fe(OH)2Cl+HCl FeOH(2+)+2Cl(-)+H2O⇔Fe(OH)2(+)+Cl(-)+H(+)+Cl(-) FeOH(2+)+H2O⇔Fe(OH)2(+)+H(+) 3 ступень Fe(OH)2Cl+H2O⇔Fe(OH)3+HCl Fe(OH)2(+)+Cl(-)+H2O⇔Fe(OH)3+H(+)+Cl(-) Fe(OH)2(+)+H2O⇔Fe(OH)3+H(+) KNO2-сильное основание,слабая кислота,гидролиз по аниону KNO2+HOH⇔KOH+HNO2 K(+)+NO2(-)+HOH⇔K(+)+OH(-)+HNO2 NO2(-)+HOH⇔HNO2+OH(-)
Так, тут потруднее будет... Давай разбираться!) Мы её решим:) И так, у нас с тобой есть раствор NaOH и кусок металла (Na). Первое что мы делаем по условию, это кидаем натрия в данный раствор и наблюдаем бурную реакцию. Дело в том, что ключевое слово в данной задачи - это раствор, а раствор = растворитель (в данном случае вода) + растворённое вещество (NaOH). Так вот, ясно, понятно, что натрий реагировать с NaOH не будет, поскольку основный металл + щелочь = реакция не идёт. Значит, натрий прореагирует с водой, с образованием той же щёлочи NaOH, а значит масса растворённого вщества будет больше, т.е образуется определённая масса NaOH, которая в сумме с уже растворённым веществом даёт новую массу. Либо, новое количество вещества. Так вот!))) Смотри:
4) n(CO2) = V(CO2) : Vm = 11,2 л. : 22,4 л/моль = 0,5 моль;
5) n(NaOH) : n(CO2) = 2,5 : 0,5 = 5 : 1 => n(NaOH) - в избытке, а значит образуется средняя соль - Na2CO3 (Карбонат Натрия). Таким образом, расчёты ведём по недостатку, т.е по n(CO2):
Ca₃PO₄+6H₂O=3Ca(OH)₂+2PH₃
2PH₃+4O₂=P₂O₅+3H₂O
P₂O₅+H₂O=2HPO₃
HPO₃+H₂O=H₃PO₄
2)3NaOH+H₃PO₄=Na₃PO₄+3H₂O
3Na(+)+3OH(-)+3H(+)+PO₄(3-)=3Na(+)+PO₄(3-)+3H₂O
3OH(-)+3H(+)=3H₂O,сокращаем на 3,получается:
OH(-)+H(+)=H₂O
2FeCl₃+3Ca(OH)₂=2Fe(OH)₃+3CaCl₂
2Fe(3+)+6Cl(-)+3Ca(2+)+6OH(-)=2Fe(OH)₃+3Ca(2+)+6Cl(-)
2Fe(3+)+6OH(-)=2Fe(OH)3,сокращаем на 2,получается:
Fe(3+)+3OH(-)=Fe(OH)3
3)NaNO3(не подвергается гидролизу,потому что образована сильной кислотой и основанием)
FeCl₃-основана слабым основанием и сильной кислотой,гидролиз идет по катиону
1 ступень
FeCl3+HOH⇔FeOHCl2+HCl
Fe(3+)+3Cl(-)+H2O⇔FeOH(2+)+2Cl(-)+H(+)+Cl(-)
Fe(3+)+H2O⇔FeOH(2+)+H(+)
2 ступень
FeOHCl2+H2O⇔Fe(OH)2Cl+HCl
FeOH(2+)+2Cl(-)+H2O⇔Fe(OH)2(+)+Cl(-)+H(+)+Cl(-)
FeOH(2+)+H2O⇔Fe(OH)2(+)+H(+)
3 ступень
Fe(OH)2Cl+H2O⇔Fe(OH)3+HCl
Fe(OH)2(+)+Cl(-)+H2O⇔Fe(OH)3+H(+)+Cl(-)
Fe(OH)2(+)+H2O⇔Fe(OH)3+H(+)
KNO2-сильное основание,слабая кислота,гидролиз по аниону
KNO2+HOH⇔KOH+HNO2
K(+)+NO2(-)+HOH⇔K(+)+OH(-)+HNO2
NO2(-)+HOH⇔HNO2+OH(-)
Так, тут потруднее будет... Давай разбираться!) Мы её решим:) И так, у нас с тобой есть раствор NaOH и кусок металла (Na). Первое что мы делаем по условию, это кидаем натрия в данный раствор и наблюдаем бурную реакцию. Дело в том, что ключевое слово в данной задачи - это раствор, а раствор = растворитель (в данном случае вода) + растворённое вещество (NaOH). Так вот, ясно, понятно, что натрий реагировать с NaOH не будет, поскольку основный металл + щелочь = реакция не идёт. Значит, натрий прореагирует с водой, с образованием той же щёлочи NaOH, а значит масса растворённого вщества будет больше, т.е образуется определённая масса NaOH, которая в сумме с уже растворённым веществом даёт новую массу. Либо, новое количество вещества. Так вот!))) Смотри:
Дано:
mр-ра(NAOH) = 200 г.
W(NaOH) = 10% = 0,1
m(Na) = 46 г.
V(CO2) = 11,2 л.
Найти:
W%(Na2CO3) - ?
(1)
1) n1(NaOH) = n(Na) = (Na) : M(Na) = 46 г : 23 г/моль = 2 моль;
2) n2(NaOH) = (mр-ра(NaOH) * W(NaOH)) : M(NaOH) = 200 г. * 0,1 : 40 г/моль = 0,5 моль;
3) n3(NaOH) = n1(NaOH) + n2(NaOH) = 2 моль + 0,5 моль = 2,5 моль;
4) n(CO2) = V(CO2) : Vm = 11,2 л. : 22,4 л/моль = 0,5 моль;
5) n(NaOH) : n(CO2) = 2,5 : 0,5 = 5 : 1 => n(NaOH) - в избытке, а значит образуется средняя соль - Na2CO3 (Карбонат Натрия). Таким образом, расчёты ведём по недостатку, т.е по n(CO2):
(2)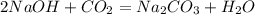
n(Na2CO3) = n(CO2) = 0,5 моль;
m(Na2CO3) = n(Na2CO3) * M(Na2CO3) = 0,5 моль * 106 г/моль = 53 г.
6) mр-ра = mр-ра(NaOH) + m(Na) - m(H2) + m(CO2) = 200 г + 46 г - 2 г + 22 г = 266 г.;
7) W%(Na2CO3) = m(Na2CO3) : mр-ра * 100% = 53 г. : 266 г. * 100% = 20%.
ответ: W%(Na2CO3) = 20%.