Практическая работа №7
Тема: «Решение экспериментальных задач»
Цель работы: опытным путем определить выданные вещества, осуществить превращения
Реактивы и оборудование: соляная кислота, гидроксид натрия, хлорид натрия, сульфат натрия, карбонат натрия, нитрат серебра, хлорид бария, пероксид водорода.
Ход работы:
Задание №1.
В трех пробирках даны растворы HCl, NaOH и NaCl. Опытным путем определите каждое вещество. Заполните таблицу.
Что делали Что наблюдали Вывод
Задание №2.
В трех пробирках даны растворы: хлорид натрия, сульфат натрия и карбонат натрия. Опытным путем определите каждое вещество. Заполните таблицу.
Что делали Что наблюдали Вывод
Задание №3.
Практически осуществить превращения
Ft FeСl2 Fe(OH)2 Fe(OH)3 → Fe2O3
Заполните таблицу.
Что делали Что наблюдали Вывод
1,12 л.
Объяснение:
1. Напишем реакцию взаимодействия цинка с раствором кислоты H2Se :
H2Se+Zn=ZnSe+H2↑ ( 1 )
2. Находим количество вещества цинка, участвующего в реакции, по формуле:
n=mM .
Молярная масса цинка M(Zn)=65г/моль,m=3,25 г.
Подставляем значения в формулу:
n=3,25г / 65 г/моль = 0,05 моль.
3. Составим и решим пропорцию. Согласно уравнению реакции ( 1 ) из 1 моль цинка получается 1 моль H2 , а из 0,05 моль получается x моль H2 . Таким образом получаем:
1моль⋅0,05моль / 1моль= 0,05 моль.
4. Вычислим объём водорода, зная, что молярный объём любого газа Vm=22,4л/моль :
V(H2)=n⋅Vm=0,05 моль⋅22,4 л/моль= 1,12 л.
Рассмотрим поочереди все реакции.
1)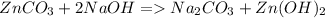
Реакция идет потому что в ходе нее образуется слабый электролит - гидроксид цинка, но углекислого газа не выделяется, так как в растворе присутствует стабильный ион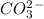 .
.
2)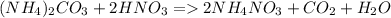
В этой реакции происходит выделение углекислого газа, поскольку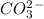 связивается с протонами
связивается с протонами 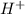 , образуя нустойчивое соединение - угольную кислоту, которая разлагается на углекислый газ и воду.
, образуя нустойчивое соединение - угольную кислоту, которая разлагается на углекислый газ и воду.
3)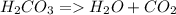
Эта реакция является иллюстрацией предыдущего процесса. Равновесие здесь смещено в сторону образования продуктов, это смещение усиливается еще больше при нагревании.
4)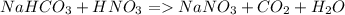
Реакция аналогична пункту 2.