При нейтрализации 296г серной кислоты гидроксидом натрия выделилось 400 г сульфата натрия. какова массовая доля (в%) выхода соли от теоретически возможного?
n = N/Nа. --> N = nNа. = 0,3 * 6,02 * = 1,806 * 10^{23}
ответ: 1,806 * молекул
5.
Дано:
N(Cu) = 1,2 * атомов
Найти: n(Cu)
n = N/Nа. = (1,2 * )/(6,02 * 10^{23}) = 0,2 моль
ответ: 0,2 моль
Формулы:
n = N/Nа. = m/M = V/Vm., где
n - количество вещества (моль), N - количество молекул/атомов, Nа. - постоянное число Авогадро (6,02 * 10^{23}), m - масса вещества (г), M - молярная масса, V - объём (л), Vm - молярный объём (22,4 л)
3. 0,4 моль
4. 1,806 * 10^{23} молекул
5. 0,2 моль
Объяснение:
3.
Дано:
N(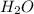 ) = 24 *
) = 24 * 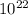
Найти: n(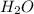 )
)
n = N/Nа. = (24 *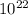 )/(6,02 *
)/(6,02 * 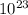 ) = 0,4 моль
) = 0,4 моль
ответ: 0,4 моль
4.
Дано:
n(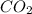 ) = 0,3 моль
) = 0,3 моль
Найти: N(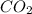 )
)
n = N/Nа. --> N = nNа. = 0,3 * 6,02 *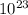 = 1,806 * 10^{23}
= 1,806 * 10^{23}
ответ: 1,806 *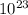 молекул
молекул
5.
Дано:
N(Cu) = 1,2 *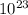 атомов
атомов
Найти: n(Cu)
n = N/Nа. = (1,2 *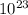 )/(6,02 * 10^{23}) = 0,2 моль
)/(6,02 * 10^{23}) = 0,2 моль
ответ: 0,2 моль
Формулы:
n = N/Nа. = m/M = V/Vm., где
n - количество вещества (моль), N - количество молекул/атомов, Nа. - постоянное число Авогадро (6,02 * 10^{23}), m - масса вещества (г), M - молярная масса, V - объём (л), Vm - молярный объём (22,4 л)
Пускай масса кислорода равна х г.
Тогда масса искомого элемента равна (х + 87,5) г.
Зная, что их сумма равна 175 г, составим уравнение:
х + (х + 87,5) = 175;
х + х + 87,5 = 175;
2х + 87,5 = 175;
2х = 175 - 87,5;
2х = 87,5;
х = 43,75 (г) — масса кислорода в оксиде.
Найдем молярную массу кислорода:
M (O₂) = 2 ∙ Ar(O) = 2 ∙ 16 = 32 (г/моль).
Значит, масса кислорода в 1 моле оксида равна 32 г.
Масса кислорода в n моль оксида равна 43,75 г.
Составим пропорцию и выразим из нее количество вещества ХО₂:
Судя по формуле соединения, 1 моль оксида содержит 1 моль неизвестного элемента, то есть n (ХО₂) = n (Х).
Формула количества вещества:
n = m : M.
Отсюда выразим молярную массу:
M = m : n.
Масса искомого элемента равна m (O₂) + 87,5 = 43,75 + 87,5 = 131,25 (г).
M (X) = m (X) : n (X) = 131,25 : 1,37 = 96 (г/моль).
Смотрим в таблице Менделеева, какой элемент имеет такую атомную массу, и это молибден (Mo). Это и есть элемент, образовавший данный оксид.
ответ: молибден (Mo).