При сжигании 156 г смеси метанола с этанолом образовалось 134,4 (н.у.) оксида углерода 4. вычислите количество вещества каждого спирта в исходной смеси. объясните как решать такие !
Так вот, такие задачки решаются системой уравнений. Смотри по - шагово:
1 - Составляем уравнению протекающих реакций:
(а)
(б)
2 - Пусть в реакцию вступит х моль метилового спирта, т.е. моль, тогда, по уравнению реакции 1, образуется x моль углекислого газа.
Пусть в реакцию вступит y моль этилового спирта, т.е. моль,
тогда, по уравнению реакции 2, образуется в 2 раза больше углекислого газа, т.е. 2y моль.
3 - Мы знаем общий объем выделившегося углекислого газа, значит мы можем найти общее количество вещества газа: = 134,4л/22,4л/моль = 6 моль
4 - Теперь, что мы делаем. Мы знаем, что в общем выделилось 6 моль газа, а из чего эти 6 моль состоят - из количества вещества CO2 в первой реакции + количество вещества CO2 во второй реакции, т.е. можно записать:
5 - Мы знаем общую массу смеси, точно так же, как и в случае с газами, масса смеси будет равна массе метанола и массе этанола. Как рассчитать массу этанола и метанола - количество вещества умножить на молярную массу, количество вещества мы установили - CH3OH - x моль, C2H5OH - y моль, значит, массы соответственно равны: - 32х - для метилового спирта и 46у - для этилового спирта.
Теперь состами уравнение и из них: 32х + 46у = 156, сократим на 2 - получим: 16х + 23у = 78
- Теперь нам нужно составить систему уравнений, так как количество вещества не может жить без массы, то мы имеем полное право таковую составить:
- Далее, решаем эту систему таким образом, сначала, верхнюю часть х + 2у = 6, умножим на 16, и вычтем из первого уравнению второе, получим уравнение такого вида: 9y = 18
y = 2
- Теперь считаем х
6 = х + 2у
6 = х +2*2
6 = х + 4
х = 2
- Помним, что х и у - заданные нами количества вещества, т.е. метиловый спирт был взят в количестве 2 моль и этиловый спирт тоже был взят в количестве 2 моль
Т.е. в ответ пойжет, то, что n(CH3OH) = 2 моль, а n(C2H5OH) = 2 моль тоже
Хорошая задачка, очень люблю такие, на смеси.
Так вот, такие задачки решаются системой уравнений. Смотри по - шагово:
1 - Составляем уравнению протекающих реакций:
(а)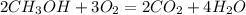
(б)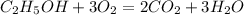
2 - Пусть в реакцию вступит х моль метилового спирта, т.е.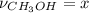 моль, тогда, по уравнению реакции 1, образуется x моль углекислого газа.
моль, тогда, по уравнению реакции 1, образуется x моль углекислого газа.
Пусть в реакцию вступит y моль этилового спирта, т.е.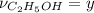 моль,
моль,
тогда, по уравнению реакции 2, образуется в 2 раза больше углекислого газа, т.е. 2y моль.
3 - Мы знаем общий объем выделившегося углекислого газа, значит мы можем найти общее количество вещества газа:
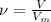 = 134,4л/22,4л/моль = 6 моль
= 134,4л/22,4л/моль = 6 моль
4 - Теперь, что мы делаем. Мы знаем, что в общем выделилось 6 моль газа, а из чего эти 6 моль состоят - из количества вещества CO2 в первой реакции + количество вещества CO2 во второй реакции, т.е. можно записать:
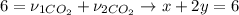
5 - Мы знаем общую массу смеси, точно так же, как и в случае с газами, масса смеси будет равна массе метанола и массе этанола. Как рассчитать массу этанола и метанола - количество вещества умножить на молярную массу, количество вещества мы установили - CH3OH - x моль, C2H5OH - y моль, значит, массы соответственно равны:
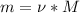 - 32х - для метилового спирта и 46у - для этилового спирта.
- 32х - для метилового спирта и 46у - для этилового спирта.
Теперь состами уравнение и из них:
32х + 46у = 156, сократим на 2 - получим:
16х + 23у = 78
- Теперь нам нужно составить систему уравнений, так как количество вещества не может жить без массы, то мы имеем полное право таковую составить:
- Далее, решаем эту систему таким образом, сначала, верхнюю часть х + 2у = 6, умножим на 16, и вычтем из первого уравнению второе, получим уравнение такого вида:
9y = 18
y = 2
- Теперь считаем х
6 = х + 2у
6 = х +2*2
6 = х + 4
х = 2
- Помним, что х и у - заданные нами количества вещества, т.е. метиловый спирт был взят в количестве 2 моль и этиловый спирт тоже был взят в количестве 2 моль
Т.е. в ответ пойжет, то, что n(CH3OH) = 2 моль, а n(C2H5OH) = 2 моль тоже