Растворы солей меди образуют со щелочами осадок Cu(OH)2, а с сероводородом - осадок CuS. Чем можно объяснить, что концен-трированный раствор сульфата тетраамминмеди (II) образует осадок с сероводородом и не образует осадка со щелочью? Напишите молеку-лярные и ионно-молекулярные уравнения указанных реакций
Комплексное соединение - сульфат тетраамминмеди (II) - диссоциирует по внешней сфере:
[Cu(NH3)4]SO4 > [Cu(NH3)4]²⁺ + SO₄²⁻
Взаимодействие комплексного соединения с гидроксидом натрия также протекает по внешней сфере:
Комплексный ион внутренней сферы комплекса при этом не разрушается, а происходит замена сульфат-ионов на гидроксид-ионы во внешней сфере.
Кроме того большое значение имеет константа нестойкости комплекса и константа диссоциации малорастворимых соединений.
Константа нестойкости комплекса [Cu(NH3)4]²⁺ равна 5·10⁻¹⁴, а константа ионизации Сu(OH)2 по первой ступени всего 2· 10⁻⁷, а по второй ступени еще меньше. Таким образом, гидроксид ионы не могут связать все ионы Сu²⁺ в нерастворимое соединении и разрушить тетраамминый комплекс меди (II).
Cероводород связывает ионы меди в малорастворимое соединение СuS (ПР 6,3· 10⁻³⁶), а также молекулы аммиака и сульфат-ионы. Внешняя и внутренняя сферы комплекса при этом разрушаются.
12
Объяснение:
Молекулярная формула воды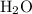 - одна молекула состоит из двух атомов водорода и одного атома кислорода. Каждый из атомов может быть одним из изотопов.
- одна молекула состоит из двух атомов водорода и одного атома кислорода. Каждый из атомов может быть одним из изотопов.
Примеры:
1) Легкая вода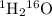 - молекулярная масса 1 + 1 + 16 = 18
- молекулярная масса 1 + 1 + 16 = 18
2) Тяжелокислородная вода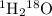 - молекулярная масса 1 + 1 + 18 = 20
- молекулярная масса 1 + 1 + 18 = 20
3) Полутяжелая вода - молекулярная масса 1 + 2 + 16 = 19
- молекулярная масса 1 + 2 + 16 = 19
Дальше я молекулярные формулы писать не буду, принцип должен быть понятен.
Сочетаний изотопов водорода 6: HH, HD, HT, DD, DT, TT (H имеет массу 1, D - 2 и T - 3) - и для каждого сочетания есть два варианта изотопа кислорода.
Всего получается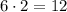 видов молекул
видов молекул
Объяснение:
Растворы солей меди образуют со щелочами осадок Cu(OH)2, а с сероводородом - осадок CuS. Чем можно объяснить, что концен-трированный раствор сульфата тетраамминмеди (II) образует осадок с сероводородом и не образует осадка со щелочью? Напишите молеку-лярные и ионно-молекулярные уравнения указанных реакций
Комплексное соединение - сульфат тетраамминмеди (II) - диссоциирует по внешней сфере:
[Cu(NH3)4]SO4 > [Cu(NH3)4]²⁺ + SO₄²⁻
Взаимодействие комплексного соединения с гидроксидом натрия также протекает по внешней сфере:
[Cu(NH3)4]SO4 + 2NaOH = [Cu(NH3)4](OH)₂ + Na2SO4
[Cu(NH3)4]²⁺ + SO₄²⁻ + 2Na⁺ + 2OH⁻ = [Cu(NH3)4]²⁺ +2OH⁻ + 2Na⁺+ SO₄²⁻
Комплексный ион внутренней сферы комплекса при этом не разрушается, а происходит замена сульфат-ионов на гидроксид-ионы во внешней сфере.
Кроме того большое значение имеет константа нестойкости комплекса и константа диссоциации малорастворимых соединений.
Константа нестойкости комплекса [Cu(NH3)4]²⁺ равна 5·10⁻¹⁴, а константа ионизации Сu(OH)2 по первой ступени всего 2· 10⁻⁷, а по второй ступени еще меньше. Таким образом, гидроксид ионы не могут связать все ионы Сu²⁺ в нерастворимое соединении и разрушить тетраамминый комплекс меди (II).
По другому протекает реакция с сероводородом:
[Cu(NH3)4]SO4 + 2H2S = CuS↓ + (NH4)2S + (NH4)2SO4
[Cu(NH3)4]²⁺ + SO4²⁻ + 2H2S = CuS↓ + 2NH4⁺ + S²⁻ + 2NH4⁺ +SO4²⁻
Cероводород связывает ионы меди в малорастворимое соединение СuS (ПР 6,3· 10⁻³⁶), а также молекулы аммиака и сульфат-ионы. Внешняя и внутренняя сферы комплекса при этом разрушаются.