3) Валентные или электроны внешних электронных оболочек, потому что они наиболее удалены от ядра. К тому же если они не заполнены полностью, такой атом вступает в хим.реакции.
4) Главная подгруппа содержит элементы малых и больших периодов, а побочная - только больших.
Также главную подгруппу составляют s- и p-элементы, а побочную подгруппу -- d-элементы.
5) В главных подгруппах с увеличением относительных атомных масс, усиливаются металлические свойства элементов.
Неметаллические свойства у элементов главных подгрупп с увеличением порядкового номера ослабевают. (у побочных наоборот)
3)Наиболее слабо связаны с ядром электроны ,расположенные на последнем энергетическом уровне,т к ядро может отдавать электроны только с внешнего уровня.А если оно может их отдавать ,то следовательно связь слабая.
4)Главная подгруппа состоит из элементов малых периодов.Побочная подгруппа состоит из элементов больших периодов.
5)Период — последовательность атомов по возрастанию заряда ядра и заполнению электронами внешнего электронного уровня.
Группа- последовательность атомов по возрастанию заряда ядра , обладающих однотипным электронным строением.
6)Металлические свойства элементов в главных подгруппах ,с увеличением относительных атомных масс, увеличиваются. А у побочных наоборот уменьшаются.
Неметаллические свойства элементов главных подгрупп с увеличением порядкового номера уменьшаются. А у побочных ,наоборот,увеличиваются.
1)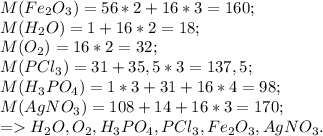
2) формула: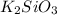
молярная масса: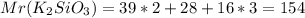
3) Валентные или электроны внешних электронных оболочек, потому что они наиболее удалены от ядра. К тому же если они не заполнены полностью, такой атом вступает в хим.реакции.
4) Главная подгруппа содержит элементы малых и больших периодов, а побочная - только больших.
Также главную подгруппу составляют s- и p-элементы, а побочную подгруппу -- d-элементы.
5) В главных подгруппах с увеличением относительных атомных масс, усиливаются
металлические свойства элементов.
Неметаллические свойства у элементов главных подгрупп с увеличением порядкового номера ослабевают. (у побочных наоборот)
1 ) H2O ; O2; H3PO4; PCI3; FE2O3; AGNO3.
2) K2SiO3 Mr=39*2+28+48=154
3)Наиболее слабо связаны с ядром электроны ,расположенные на последнем энергетическом уровне,т к ядро может отдавать электроны только с внешнего уровня.А если оно может их отдавать ,то следовательно связь слабая.
4)Главная подгруппа состоит из элементов малых периодов.Побочная подгруппа состоит из элементов больших периодов.
5)Период — последовательность атомов по возрастанию заряда ядра и заполнению электронами внешнего электронного уровня.
Группа- последовательность атомов по возрастанию заряда ядра , обладающих однотипным электронным строением.
6)Металлические свойства элементов в главных подгруппах ,с увеличением относительных атомных масс, увеличиваются. А у побочных наоборот уменьшаются.
Неметаллические свойства элементов главных подгрупп с увеличением порядкового номера уменьшаются. А у побочных ,наоборот,увеличиваются.