СДЕЛАЙТЕ СОР 7.3А Простые химические реакции,7.3В Периодическая таблица химических элементов, 7.3С Относительная атомная масса. Простейшие формулы.
Пользуясь фрагментом периодической системы химических элементов Д.И. Менделеева выберите ряд элементов ОДНОГО ПЕРИОДА: *
Li, Na, Mg
Li, Na, Rb
B, F, Ar
Li, C, O
O, F, Cl
Перечислены вещества, обладающие природной кислотностью и мылкостью. На основании бытовых знаний определите КИСЛОТЫ *
чистящее средство "комет"
лимонная кислота
стиральный порошок,
яблочный уксус
аспирин
Пользуясь фрагментом периодической системы химических элементов Д.И. Менделеева выберите ряд элементов ОДНОЙ ГРУППЫ : *
Li, Na, Mg
Li, Na, Rb
B, F, Ar
Li, C, O
O, F, Cl
Предположите, как будут реагировать с разбавленными кислотами следующие металлы: *
натрий
медь
свинец
С разбавленными кислотами не реагирует
Бурно реагирует с разбавленными кислотами с выделением газа
Реагирует с разбавленными кислотами менее интенсивно с выделением газа
С разбавленными кислотами не реагирует
Бурно реагирует с разбавленными кислотами с выделением газа
Реагирует с разбавленными кислотами менее интенсивно с выделением газа
Выберите вариант ответа в каждой строке.
Даны 3 пробирки. В пробирку под №1 прилили индикатор фенолфталеин, раствор был прозрачный, стал малиновый. В пробирку №2 прилили лакмус, раствор стал красным. В пробирку №3 прилили метиловый оранжевый, раствор изменил цвет на желтый. Определите какие вещества находились в пробирках №1 №2 №3? *
№1 щелочь, №2 кислота,№3 щелочь
№1 кислота, №2 щелочь, №3 кислота
№1 щелочь ,№2 кислота, №3 кислота
Рассчитайте относительные молекулярные массы соединений. Mr (H2SO3) = *
Мой ответ
Отметьте фактор, доказывающий, что выделяющийся газ – водород: *
а)Тлеющая лучинка загорается
b)Горящая лучинка гаснет
c)Наблюдается помутнение раствора
d)Сгорает со звуком «пах»
e) Появляется резкий запах
Составьте формулу бинарного соединения, исходя из названий химических элементов, валентности и их атомных соотношений: C (IV) H (I) *
Мой ответ
Современная классификация химических элементов разработана усилиями многих учёных, в числе которых был Ньюлендс. Объясните принцип классификации химических элементов Ньюлендса *
Мой ответ
Перечислены вещества, обладающие природной кислотностью и мылкостью. На основании бытовых знаний определите ЩЕЛОЧИ *
аспирин
яблочный уксус
стиральный порошок
лимонная кислота
чистящее средство "комет"
Определите, что произойдет с горящей лучиной, если ее поднести к сосуду с газированной минеральной водой *
Мой ответ
Составьте формулу бинарного соединения, исходя из названий химических элементов, валентности и их атомных соотношений: N (III) и O (II) *
Мой ответ
Какая реакция происходит между кислотой и основанием *
Мой ответ
Напишите словесное уравнение взаимодействие соляной кислоты с карбонатом натрия. *
Мой ответ
Назовите недостатки классификации И.Дёберейнера *
Мой ответ
Напиши словесное уравнение химической реакции взаимодействия ГИДРОКСИДА НАТРИЯ И АЗОТНОЙ КИСЛОТЫ *
Мой ответ
Кожний енергетичний рівень складається з орбіталей певної форми: перший містить одну s-орбіталь, другий — s- і р-орбіталі, третій — s-, р-, d-орбіталі. Отже, зверни увагу: який номер рівня, стільки й форм орбіталей, що його утворюють.
Число орбіталей на енергетичних рівнях різне, воно дорівнює n2, де n — номер рівня. На першому рівні (n = 1) одна 8-орбіталь, на другому (n = 2) — чотири: одна s- і три р-орбіталі, на третьому (n = 3) — дев'ять: одна три р- і п'ять d-орбіталей Зважаючи на те, що на кожній з орбіталей може перебувати не більше двох електронів, максимальна кількість електронів на тому чи іншому енергетичному рівні дорівнює 2n2
Найважливіші характеристики орбіталей (енергія, форма, розміщення в просторі) визначаються квантовими числами.
ЕСЛИ ЕСТЬ ВОПРОС пиши в комментарий отвечу
Объяснение:M(Mn3(PO4)2 * 6H2O = (Mn*3)+(P*2)+(O*8)+(H2O*6) = г/моль
M(Mn3(PO4)2 * 6H2O = (55*3)+(31*2)+(16*8)+(18*6) = 463 г/моль
W(Mn3(PO4)2)=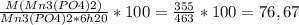 %
%
W(H2O) = 100% - 76,76%=23,24%
M(CaCO3 * 8H2O) = 40 + 12 + 48 +(18*6)=208 г/на моль
W(CaCO3) =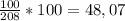 %
%
W(H2O) = 100 - 48,07 = 51,93%
M(FeSO3*O,5H2O) =56+32+(16*3)+(18*0,5)=145 г/моль
W(FeSO3) =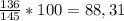 %
%
w(H2O) = 100% - 88,31% =11,69%
3. Очень простая задача) Формула мідного купоросу - CuSO4*5H2O
M(CuSO4*5H2O) = 160 + 18*5= 160+90 = 250г/моль
W(CuSO4) =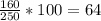 %
%
m(CuSO4)=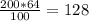 г
г