"Энергия ионизации для элементов одного периода возрастает слева направо с возрастанием заряда ядра. В подгруппе она уменьшается сверху вниз вследствие увеличения расстояния электрона от ядра. Изменение энергии ионизации атомов с ростом заряда ядра графически представлено на рис. Энергия ионизации связана с химическими свойствами элементов. Так, щелочные металлы, имеющие небольшие энергии ионизации, обладают ярко выраженными металлическими свойствами. Химическая инертность благородных; газов связана с их высокими j значениями энергии ионизации. Атомы могут не только отдавать, но и присоединять электроны. При этом образуется соответствующий анион. Энергия, которая выделяется при присоединении к атому одного электрона, называется сродством к электрону. Обычно сродство к электрону, как и энергия ионизации, выражается в электрон-вольтах. Значения сродства к электрону известны не для всех элементов; измерять их весьма трудно. Наиболее велики они у галогенов, имеющих на внешнем уровне по 7 электронов. Это говорит об усилении неметаллических свойств элементов по мере приближения к концу периода. Определение электроотрицательности дал американский' ученый Л. Полинг в 1932 г. Он же предложил и первую шкалу элёктроотрицательности. Согласно Полингу, электроотрицательность есть атома в соединении притягивать к себе электроны. Имеются в виду валентные электроны, т. е. электроны, которые участвуют в образовании химической связи. Очевидно, у благородных газов электроотрицательность отсутствует, так как внешний уровень в их атомах завершен и устойчив. Сопоставляя значения электроотрицательностей элементов от франция (0,86) до фтора (4,10), легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе — уменьшается. Ее значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. "
Li-5,4; Cs-3,9; Cu-7,7; Ag-9,2. Таким образом, наиболее типичным представителем металла в данном ряде будет Li - элемент обладающей наименьшей электроотрицательностью, что и определяет свойства металлов: они химически очень активны, причем их активность возрастает от Li к Fr.
В круглых скобках указано название вещества ()
1)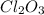 (оксид хлора(3)); Валентность: у хлора - 3, у кислорода - 2.
(оксид хлора(3)); Валентность: у хлора - 3, у кислорода - 2.
2)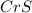 (сульфид хрома(2)); Валентность: у хрома 2, у серы 2, поэтому индексы не нужны.
(сульфид хрома(2)); Валентность: у хрома 2, у серы 2, поэтому индексы не нужны.
3)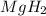 (гидрид магния); Валентность: у магния 2, у водорода - 1.
(гидрид магния); Валентность: у магния 2, у водорода - 1.
4)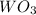 (оксид вольфрама(3)); Валентность: у вольфрама - 6, у кислорода 2.
(оксид вольфрама(3)); Валентность: у вольфрама - 6, у кислорода 2.
5)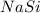 (силицид натрия); Валентность: у натрия - 1, у кремния - 1.
(силицид натрия); Валентность: у натрия - 1, у кремния - 1.
6)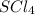 (хлорид серы(4)); Валентность: у серы - 4, у хлора 1.
(хлорид серы(4)); Валентность: у серы - 4, у хлора 1.
7)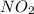 (оксид азота(4)); Валентность: у азота - 4, у кислорода - 2.
(оксид азота(4)); Валентность: у азота - 4, у кислорода - 2.
8)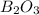 (оксид брома); Валентность: у брома - 3, у кислорода - 2.
(оксид брома); Валентность: у брома - 3, у кислорода - 2.
Учебник химии гласит:
"Энергия ионизации для элементов одного периода возрастает слева направо с возрастанием заряда ядра. В подгруппе она уменьшается сверху вниз вследствие увеличения расстояния электрона от ядра. Изменение энергии ионизации атомов с ростом заряда ядра графически представлено на рис.
Энергия ионизации связана с химическими свойствами элементов. Так, щелочные металлы, имеющие небольшие энергии ионизации, обладают ярко выраженными металлическими свойствами. Химическая инертность благородных; газов связана с их высокими j значениями энергии ионизации.
Атомы могут не только отдавать, но и присоединять электроны. При этом образуется соответствующий анион. Энергия, которая выделяется при присоединении к атому одного электрона, называется сродством к электрону. Обычно сродство к электрону, как и энергия ионизации, выражается в электрон-вольтах. Значения сродства к электрону известны не для всех элементов; измерять их весьма трудно. Наиболее велики они у галогенов, имеющих на внешнем уровне по 7 электронов. Это говорит об усилении неметаллических свойств элементов по мере приближения к концу периода.
Определение электроотрицательности дал американский' ученый Л. Полинг в 1932 г. Он же предложил и первую шкалу элёктроотрицательности. Согласно Полингу, электроотрицательность есть атома в соединении притягивать к себе электроны.
Имеются в виду валентные электроны, т. е. электроны, которые участвуют в образовании химической связи. Очевидно, у благородных газов электроотрицательность отсутствует, так как внешний уровень в их атомах завершен и устойчив.
Сопоставляя значения электроотрицательностей элементов от франция (0,86) до фтора (4,10), легко заметить, что относительная электроотрицательность подчиняется периодическому закону: в периоде она растет с увеличением номера элемента, в группе — уменьшается. Ее значения служат мерой неметалличности элементов. Очевидно, чем больше относительная электроотрицательность, тем сильнее элемент проявляет неметаллические свойства. "
Li-5,4; Cs-3,9; Cu-7,7; Ag-9,2.
Таким образом, наиболее типичным представителем металла в данном ряде будет Li - элемент обладающей наименьшей электроотрицательностью, что и определяет свойства металлов: они химически очень активны, причем их активность возрастает от Li к Fr.