Смесь составом Х205 и Х2О3 массой 61,4 г, где массовая доля кислорода 49,5%, прореагировала с кислородом и образовалось одно сложное вещество массой 71 г. Определите массу одного моля ХНз-
Найдем количество молей гидроксида меди. Количество вещества находится по формуле: , где m - масса вещества, M - молярная масса.
Молярная масса вещества находится из периодической таблицы, как сумма молярных масс входящих в него элементов.
Исходя из уравнения реакции для получения 0,1 моля гидроксида меди (II) должно быть использовано 0,2 моля гидроксида натрия и 0,1 моля сульфата меди (II).
т.е. потребуется 0,1 * (64+32 + 4 *16) = 16г сульфата меди (II) и
0,2 * (23 +16 + 1) = 8г гидроксида натрия.
Но гидроксид натрия дан в растворе. Масса раствора равна
Уравнение реакции:
Найдем количество молей гидроксида меди. Количество вещества находится по формуле: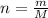 , где m - масса вещества, M - молярная масса.
, где m - масса вещества, M - молярная масса.
Молярная масса вещества находится из периодической таблицы, как сумма молярных масс входящих в него элементов.
Исходя из уравнения реакции для получения 0,1 моля гидроксида меди (II) должно быть использовано 0,2 моля гидроксида натрия и 0,1 моля сульфата меди (II).
т.е. потребуется 0,1 * (64+32 + 4 *16) = 16г сульфата меди (II) и
0,2 * (23 +16 + 1) = 8г гидроксида натрия.
Но гидроксид натрия дан в растворе. Масса раствора равна![\frac{8[g]}{0,04}=200[g]](/tpl/images/0923/0635/d3a92.png)
Находим массу соли: m Ме₂(SО₄)₃= m р-ра *W=19,6*0,2=3,92 г
Соль диссоциирует:
Ме₂(SО₄)₃= 2Ме³⁺ +3 SО₄²⁻ ( соотношение по ур 1:2:3)
х- количество Ме2(SО4)3, 2х- количество Ме³⁺, 3х – количество SО₄²⁻
Сколько моль катионов и анионов n=3,01*10^22/6,02*10^23=0,05 моль
2х+3х=0,05
5х=0,05
х=0,01 моль Ме2(SО4)3, находим молярную массу соли
М= m/ n=3,92/0,01=392 г/моль, обозначаем атомный вес Ме через х и составляем уравнение нахождения молярной массы соли( Ar(S)=32, Ar(О)=16)
392=2х+3*(32+16*4)
104=2х
х=52 это атомный вес Ме , хром.