ть Укажіть метал, з яким не може взаємодіяти розбавлена сульфатна
кислота:
А. Zn; Б. Mg; В. Hg Г. Pb
2. Виберіть властивості вуглекислого газу:
А. Газ легший за повітря, без запаху
Б. Газ важчий за повітря, з різким
запахом
В. Газ важчий за повітря, без запаху
Г. Газ легший за повітря, з різким
запахом
3. Якщо аміак пропустити крізь воду, то реакція середовища змінюється з:
А. нейтральної на лужну;
Б. нейтральної на кислу;
В. лужної на кислу.
Г. не зміниться
4. Які речовини утворюються при взаємодії концентрованої нітратної
кислоти з міддю? Напишіть відповідне рівняння реакції.
А. Cu(NO3)2 + NO↑+ H2O;
Б. Cu(NO3)2 + NO2↑+ H2O;
В. Cu(NO3)2 + H2O;
Г. Cu(NO3)2 + H2.
5. Якісна реакція на хлорид-іон – це ... (Напишіть відповідне рівняння
реакції)
А. Дія розчинних солей Арґентуму;
Б. Дія сильних кислот;
В. Дія розчинних солей Барію;
Г. Дія індикатора.
6. В одній пробірці міститься розчин сульфатної кислоти, в іншій —
хлоридної. Як розпізнати, де яка кислота міститься? Напишіть відповідні
рівняння реакцій.
7. Що таке кислотні дощі? Які негативні наслідки вони спричиняють? Як їх
уникнути?
8. Охарактеризуйте фізичні та хімічні властивості сульфатної кислоти.
Напишіть відповідні хімічні рівняння.
9. Допишіть рівняння реакцій:
А. S + O2 →
Б. Cl2 + H2 →
В. SO3 + H2O →
Г. N2 + Ca →
10. Напишіть рівняння реакцій, що лежать в основі схеми:
а) NH4Cl -NH3 -NO -NO2 -HNO3 -Mg(NO3)2
б) S -FeS -Н2S -SО2 -SО3 -ВаSО4
11*. Обчисліть масу середньої солі, яка утвориться при взаємодії
сульфур(ІV) оксиду з натрій гідроксидом масою 120 г.
2)ковалентная полярная
3) NO
4)
Количество аммиака = 1кг / (14+3) кмоль/кг = 58,82 моль
N₂ + 3H₂ --> 2NH₃
По реакции для этого необходимо минимум: 58,82/2 = 29,41 моль азота, что составляет 22,4*29,41 = 658,82 л
5)Добавление вещества с анионом OH⁻ (щелочь), при этом выделяется едкий газ (аммиак):
KOH + NH₄Cl --> KCl + NH₃ + H₂O
6) Оксид азота NO₂ (диоксид азота) — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NO₂ находится в смеси с его бесцветным димером N₂O₄, приблизительно 1:1.
Взаимодействует с водой:
2NO₂ + Н₂О = HNO₃ + HNO₂
и растворами щелочей:
2NO₂ + 2NaOH = NaNO₃ + NaNO₂ + H₂О
Сильный окислитель. Многие вещества (угол, фосфор, органические соединения) могут гореть в NO₂. Этот оксид окисляет SO₂ до SO₃. Раздражает дыхательные пути, при больших концентрациях появляется отек легких.
7) Азот может образовывать несколько типов кислот: азотная, азотистая и азотистоводородная. Соответственно их соли: нитраты (KNO₃, Cu(NO₃)₂), нитриты (KNO₂, Ca(NO₂)₂) и азиды (KN₃, AgN₃)
1.кислородсодержащие органические соединения, в которых атом Водорода, замещен на одну карбоксильную группу, называются предельные одноосновные кислоты.
2.муравьиную кислоту можно получить действием на ее соли более сильными кислотами,например,серной.А ее соль можно получить,пропуская угарный газ через нагретую щелочь
3.Фенол обладает следующими физическими свойствами:бесцветное кристаллическое вещество со специфическим запахом,температурой плавления 42,3 градуса по Цельсию,температурой кипения 181,1 градуса,довольно трудно растворим в воде,на воздухе окисляется(краснеет) и кристаллы его расплываются.
4.область применения формальдегида:в производстве пластмасс,в кожевенном деле для дубления кожи,медицине и санитарии - для дезинфекции,40%-водный раствор называют формалином и применяют в семеноводстве для протравливания зерна от грибковых заболеваний
№2 составить формулу: 3-этилгептаналь:
7 6 5 4 3 2 1
| |
№3 закончить уравнение следующих реакций, укажите условия протекания, назовите вещества:
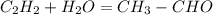 (в присутствии раствора сульфата ртути)- реакция Кучерова
(в присутствии раствора сульфата ртути)- реакция Кучерова
С2Н2--->СН3СОН--->С2Н5ОН--->НСООС2Н5
1)
2)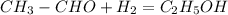 (в присутствии никеля)
(в присутствии никеля)
3)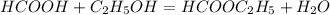 (при незначительном нагревании в присутствии концентрированной серной кислоты)
(при незначительном нагревании в присутствии концентрированной серной кислоты)