Технічний кальцій карбід масою 1.6 г залили надлишком води. під час пропускання утвореного газу крізь розчин брому в реакцію вступив бром масою 7,2 г. обчисліть масову частку домішок у технічному кальцій карбіді
Ионы это когда атомы отдают или получают один, два атома для того, чтобы приблизится к благородным газам. Эти благородные газы имеют 8 атомов во внешнем пути, эти 8 атомов на внешнем уровне - цель всех атомов. Давай расмотрим на примере Натрия и Хлора.
У натрия и три уровня, во внешнем 1 атом, во втором 8. ЧТобы стать благородным он должен избавится от этого одного атома. У хлора тоже три уровня, однако на внешнем уровне 7 атомов, то есть чтобы стать благородным ему нужен только один атом. При их соединении атом натрия отдаст свой внешний уровень хлору, благодаря чему тот кто отдал станет положительно заряженым, тот кто взял отрицательно.
Ионная связь может быть ТОЛЬКО МЕЖДУ металлами и неметаллами. То есть таковыми могут быть соеденения О, KCl
Ионы это когда атомы отдают или получают один, два атома для того, чтобы приблизится к благородным газам. Эти благородные газы имеют 8 атомов во внешнем пути, эти 8 атомов на внешнем уровне - цель всех атомов. Давай расмотрим на примере Натрия и Хлора.
У натрия и три уровня, во внешнем 1 атом, во втором 8. ЧТобы стать благородным он должен избавится от этого одного атома. У хлора тоже три уровня, однако на внешнем уровне 7 атомов, то есть чтобы стать благородным ему нужен только один атом. При их соединении атом натрия отдаст свой внешний уровень хлору, благодаря чему тот кто отдал станет положительно заряженым, тот кто взял отрицательно.
Ионная связь может быть ТОЛЬКО МЕЖДУ металлами и неметаллами. То есть таковыми могут быть соеденения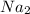 О, KCl
О, KCl
Дано:
m(H2S)=74 г
m( Fe(OH)3 )=97г
Найти:
n(Fe2S3)-?
m(Fe2S3)-?
3H2S + 2Fe(OH)3 = 6H2O + Fe2S3↓
1)Найдём количество вещества H2S:
n(H2S) = m/Mr = 74г/34г/моль=2,18 моль
Mr(H2S)=1*2+32=34 г/моль
2)Найдем количество вещества Fe(OH )3:
n( Fe(OH )3 ) = m/Mr = 97г / 110г/моль = 0,9 моль
Mr( Fe(OH )3 ) = 56+ 18*3 = 110 г/моль
3) H2S в избытке, значит расчёт ведём по Fe(OH )3:
(соотнесём количество вещества и коэффициенты)
0,9 моль/2=х/1
х=0,45 моль - количество вещества Fe2S3
4)Найдём массу Fe2S3:
m= n*Mr = 0,45 моль * 208 г/моль = 93,6 г
Mr(Fe2S3) = 56*2 + 32*3 =208 г/моль
n(Fe2S3) - 0,45 моль
m(Fe2S3) - 93,6 г
Объяснение: