Поехали. Как видно тема хим. реакции, ну чтож, попробуем.
Реакции замещения - есть реакциивзаимодействия простого и сложного вещества и простое вещество будет вытеснять ондо из состава сложного.
Реакции замещения с кислотами:
Zn + 2HCl = ZnCl2 + H2
Правило, которое очень важно при реакциях металлов с кислотами - при взаимодействии активного металла с кислотой будет вытесняться водород. ВОДОРОД, именно водород, а не кислотный остаток. Но, есть одно но. Катион водорода, будут вытеснять - замещать только активные металлы, т.е. металлы которые стоят в ряду активности до водорода, это:
натрий, калий, рубидий, цезий, железо, никель, кобальт, алюминий...все кроме - меди, серебра, золота, ртути и платины.
И еще одно правило. Из азотной кислоты водород никогда не вытесняется. Будет выделятся газ - NO, NO2 или аммиак или соли аммония, тогда речь уже будет идти об окислительно - восстановительной реакции, а не о реакции замещения.
Вот примеры реакций замещения с кислотами:
2Na + H2SO4 = Na2SO4 + H2
Mg + 2HCl = MgCl2 + H2
2Al + 6HBr = 2 AlBr3 + 3H2
Реакции замещения протекающие между простым веществом и солью.
Правило: простое вещество - металл, будет вытеснять из соли соответственно металл, но если он, в ряду активности металлов стоит правее него, т.е. слабее
Т.е. из солей будет вытесняться металл, но если он будет правее в ряду активности
Примеры:
Fe + CuSO4 = FeSO4 + Cu - медь слабее чем железо, значит железо сможет вытеснить его из соли
А вот такая реакция:
Cu + FeSO4 =/= не пойдет, медь слабее железа и не сможет его вытеснить.
Теперь алгоритм составления реакций соединения:
- Смотрим на уравнение:
Ni + HCl =
- Оцениваем силу металла. Если он стоит в ряду активности до водорода, значит пойдет реакция замещения. Если нет, значит нет.
Ni - металл стоящий до водорода, значит имеет место быть реакция замещения.
- Оцениваем кислоту. Если у нас любая кислота, кроме азотной, значит идет реакция замещения. HCl - таковой не является, значит идет реакция замещения.
- Чего заместить? Как я писал выше, металл будет вытеснять водород.
- Пишем реакцию:
Ni + HCl = NiCl2 + H2
- Уравниваем ее:
Ni + 2HCl = NiCl2 + H2
Разложения:
Это такие реакции, в ходе которых идет образование более простых веществ из более сложных. К таким реакциям можно отнести - электролиз, гидролиз, пиролиз и т.п.
Конкретно, о разложении.
Разложению подвергается одно - сложное вещество. Чаще всего разлагаются - слабые элетролиты - это нерастворимые соли и основания.
Конкретно о солях.
Соли разлагаются на два оксида. На оксид металла, который входит в соль и оксид неметалла,к который входит в кислотный остаток. Пример:
CaCO3 = CaO + H2O
Основания разлагаются на оксид соответствующий металлу в составе основания и на воду.
Пример:
Cu(OH)2 = CuO + H2O
Алгоритм реакции:
- смотрим на уравнение:
BaSO4 =t= ... + ...
- Сразу определяем, какое вещество у нас - растворимое или нет. Для этого есть таблица растворимости.
Определили - BaSO4 - нерастворимая соль, значит распадается при нагревании:
- Определяем, что за металл входит в состав соли - Ba, определяем его оксид, для этого, смотрим на группу, в которой он находится - 2группа, смотрим какой оксид соответствует элементам этой группы - RO - значит оксид бария - BaO
- Кислотный остаток. У него мы отнимаем один кислород и получим тот самый оксид:
Поехали. Как видно тема хим. реакции, ну чтож, попробуем.
Реакции замещения - есть реакциивзаимодействия простого и сложного вещества и простое вещество будет вытеснять ондо из состава сложного.
Реакции замещения с кислотами:
Zn + 2HCl = ZnCl2 + H2
Правило, которое очень важно при реакциях металлов с кислотами - при взаимодействии активного металла с кислотой будет вытесняться водород. ВОДОРОД, именно водород, а не кислотный остаток. Но, есть одно но. Катион водорода, будут вытеснять - замещать только активные металлы, т.е. металлы которые стоят в ряду активности до водорода, это:
натрий, калий, рубидий, цезий, железо, никель, кобальт, алюминий...все кроме - меди, серебра, золота, ртути и платины.
И еще одно правило. Из азотной кислоты водород никогда не вытесняется. Будет выделятся газ - NO, NO2 или аммиак или соли аммония, тогда речь уже будет идти об окислительно - восстановительной реакции, а не о реакции замещения.
Вот примеры реакций замещения с кислотами:
2Na + H2SO4 = Na2SO4 + H2
Mg + 2HCl = MgCl2 + H2
2Al + 6HBr = 2 AlBr3 + 3H2
Реакции замещения протекающие между простым веществом и солью.
Правило: простое вещество - металл, будет вытеснять из соли соответственно металл, но если он, в ряду активности металлов стоит правее него, т.е. слабее
Т.е. из солей будет вытесняться металл, но если он будет правее в ряду активности
Примеры:
Fe + CuSO4 = FeSO4 + Cu - медь слабее чем железо, значит железо сможет вытеснить его из соли
А вот такая реакция:
Cu + FeSO4 =/= не пойдет, медь слабее железа и не сможет его вытеснить.
Теперь алгоритм составления реакций соединения:
- Смотрим на уравнение:
Ni + HCl =
- Оцениваем силу металла. Если он стоит в ряду активности до водорода, значит пойдет реакция замещения. Если нет, значит нет.
Ni - металл стоящий до водорода, значит имеет место быть реакция замещения.
- Оцениваем кислоту. Если у нас любая кислота, кроме азотной, значит идет реакция замещения. HCl - таковой не является, значит идет реакция замещения.
- Чего заместить? Как я писал выше, металл будет вытеснять водород.
- Пишем реакцию:
Ni + HCl = NiCl2 + H2
- Уравниваем ее:
Ni + 2HCl = NiCl2 + H2
Разложения:
Это такие реакции, в ходе которых идет образование более простых веществ из более сложных. К таким реакциям можно отнести - электролиз, гидролиз, пиролиз и т.п.
Конкретно, о разложении.
Разложению подвергается одно - сложное вещество. Чаще всего разлагаются - слабые элетролиты - это нерастворимые соли и основания.
Конкретно о солях.
Соли разлагаются на два оксида. На оксид металла, который входит в соль и оксид неметалла,к который входит в кислотный остаток. Пример:
CaCO3 = CaO + H2O
Основания разлагаются на оксид соответствующий металлу в составе основания и на воду.
Пример:
Cu(OH)2 = CuO + H2O
Алгоритм реакции:
- смотрим на уравнение:
BaSO4 =t= ... + ...
- Сразу определяем, какое вещество у нас - растворимое или нет. Для этого есть таблица растворимости.
Определили - BaSO4 - нерастворимая соль, значит распадается при нагревании:
- Определяем, что за металл входит в состав соли - Ba, определяем его оксид, для этого, смотрим на группу, в которой он находится - 2группа, смотрим какой оксид соответствует элементам этой группы - RO - значит оксид бария - BaO
- Кислотный остаток. У него мы отнимаем один кислород и получим тот самый оксид:
SO3 - соответствует - SO3
- Пишем уравнение:
BaSO4 =t= BaO + SO3
Так, сначала условные обозначения:
1 - Определим на сколько грамм увеличили массу раствора:
250 + 32 = 285г - мы сложили массу добавленной воды и массу добавленной соли
2 - Рассчитаем массу получившегося раствора:
3 - Определим массу вещества в растворе:
m = = 315*0,15 =47,25г
= 315*0,15 =47,25г
4 - Рассчитаем на сколько стало вещества в полученном растворе, ведь помимо воды, мы добаваляем и вещества:
m(получ) =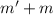 = 35г + 47,25г = 82,25г
= 35г + 47,25г = 82,25г
5 - Считаем массовую долю:
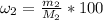 = 82,25/600*100% = 13,7%
= 82,25/600*100% = 13,7%