Задания суммативного оценивания за 1 четверть ХИМИЯ 8 класс
1. (а) Определите электронную формулу, соответствующую иону S -2 .
А) 1s 2 2s 2 2p 6 3s 2 3p 5
B) 1s 2 2s 2 2p 6 3s 2 3p 6
C) 1s 2 2s 2 2p 6
D) 1s 2 2s 2 2p 6 3s 2 3p 4
[1]
(b) Определите строку, в которой схема распределения электронов соответствует атому неона.
А) F о , 1s 2 2s 2 2p 5
B) Na + , 1s 2 2s 2 2p 6 3s 1
C) Na +1 , 1s 2 2s 2 2p 6
D) Cl +5 , 1s 2 2s 2 2p 6 3s 2
[1]
2 (а) Элемент, который образует ион с зарядом Э -3 , присоединяет электроны на третий
энергетический уровень. Составьте формулу его соединения с водородом:
ответ
[1]
2 (b) Закончите схему образования иона Cl +7 .
[1]
3. Напишите электронную и электронно – графическую формулы атома алюминия:
Электронная формула:
Электронно – графическая формула:
[2]
4. Азот может образовывать пять оксидов разного состава. Составьте формулу оксида
азота методом «нулевой суммы».
N +5 x O -2 y
[1]
5. Рассчитайте массовую долю азота в получившемся оксиде азота в задании 4.
[2]
6. Определите и подпишите тип химической реакции.
Химическая реакция Тип реакции
2KBr + Cl 2 = 2KCl + Br 2
AgNO 3 + KBr = AgBr + KNO 3
PbO + SiO 2 = PbSiO 3
[1]
7. (a) На рисунке изображены реакции взаимодействия
металлов с кислотой:
Пробирка №1 – реакция протекает бурно, с выделением
большого количества газообразного вещества;
Пробирка №2 – реакция протекает активно, наблюдается
выделение газообразного вещества;
Пробирка №3 – протекание реакции не наблюдается.
Задание:
Предложите по одному примеру металлов для реакции в
пробирках 1 и 2:
Пробирка №1
Пробирка №2 [1]
(b) Напишите уравнение реакции взаимодействия кислоты с предложенными вами
металлами для пробирок № 1 и 2 в задании 7(a).
[2]
8. Для исследования активности металла ученик поместил никель в разные растворы.
(а) Заполните таблицу, поставив «+» и «-» в соответствие с возможностью
или отсутствием реакции:
AgNO 3 HCl ZnSO 4 H 2 O(пар)
Ni
[1]
(b) Объясните причину подобного химического поведения никеля.
[2]
9.Выбери из перечня только те металлы, которые реагируют с соляной кислотой и напиши
соответствующие уравнения реакции: Ca , Ag, Al, Au, Na.
[3]
10.Допишите уравнения только тех реакций, которые практически осуществимы и
уравняйте правую и левую часть:
Fe + CuSO 4 =
Al + FeSO 4 =
CuCl 2 + Mg =
Cu + MgSO 4 =
Mg + CuSO 4 =
Hg + ZnSO 4 =
[6]
Итого
C2H5Br + NaOH = C2H5OH + NaBr
C2H5OH + CH3COOH ---(H2SO4)---> CH3COOC2H5 + H2O
CH3COOC2H5 + NaOH = CH3COONa + C2H5OH
CH3COONa + NaOH + t (сплав) = CH4 + Na2CO3 CH4 + t = C2H2
C2H2 + HCl = CH2=CH-Cl nCH2=CH-Cl = [-CH2-CH(Cl)-]n
2. CH3COOCH3 ---(NaOH/H2O)---> CH3COONa + CH3OH
CH3OH + O2 ---(V2O5/t)---> HCOH + H2O
HCOH + [Ag(NH3)2]OH = Ag + HCOOH + H2O + 2NH3
HCOH ---(H2/Ni)---> CH3OH
CH3OH + C2H5COOH ---(H2SO4)---> C2H5COOCH3 + H2O
C2H5COOCH3 + NaOH (водн) = C2H5COONa + CH3OH
C2H5COONa + NaOH + t (сплав) = C2H6 + Na2CO3
3. C3H7OH ---(Cu/t)---> C2H5CHO + H2
C2H5CHO + Cu(OH)2 = C2H5COOH + Cu2O
C2H5COOH + C2H5OH ---(H2SO4)---> C2H5COOC2H5
C2H5COOC2H5 + NaOH (водн) = C2H5COONa + C2H5OH
1) Уравняем схему рекации:
Из чего можно сделать вывод о том, что KCl образуется столько же, сколько KClO3 было. А O2 в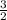 раза больше, поэтому.
раза больше, поэтому.
2) 3 Ba + 2 H3PO4 → 3 H2 + Ba3(PO4)2
Бария столько же, сколько и водорода, следовательно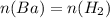
Фосфорной кислоты 3/4 от количества водорода
3) Поскольку 4,8% примесей, то
1000г*0,048=48 грамм примесей.
Тогда чистого железа
1000 - 48 = 952 г.
Fe+H2SO4 => FeSO4 + H2
n(Fe)=m/M=952/56=17 моль
Соли образуется столько же, сколько и железа было
n(Fe)=n(FeSO4)
m(FeSO4)=n*M = 17*152 = 2584 г
Водорода образуется столько же, поэтому
n(Fe)=n(H2)
V(H2)=n*Vm = 17* 22,4 = 380,8 л.