Дано:
n(Zn) = 0,2 моль
Найти:
m(Zn) - ?
n = ⇒ m = n * M
M(Zn) = Ar(Zn) = 65 г/моль
m(Zn) = 0,2 моль * 65 г/моль = 13 г.
N(MgO) = 3 * 10²³ частиц
m(MgO) - ?
n(MgO) - ?
n(MgO) = = ≈ 0,5 моль
m(MgO) = n * M
M(MgO) = Ar(Mg) + Ar(O) = 24 * 16 = 40 г/моль
m(MgO) = 0,5 моль * 40 г/моль = 20 г.
m(CO₂) = 22 г.
n(CO₂) - ?
N(CO₂) - ?
n(CO₂) =
M(CO₂) = Ar(C) + Ar(O) * 2 = 12 + 16 * 2 = 12 + 32 = 44 г/моль
n(CO₂) = 22 г. / 44 г/моль = 0,5 моль
N(CO₂) = n * N = 0,5 моль * 6,02 * 10²³ моль⁻¹ = 3,01 * 10²³ частиц
N(Br₂) = 12 * 10²³ частиц
m(Br₂) - ?
n(Br₂) - ?
n(Br₂) = = ≈ 2 моль
m(Br₂) = n * M
M(Br₂) = Ar(Br) * 2 = 80 * 2 = 160 г/моль
m(Br₂) = 2 * 160 = 320 г.
m(H₂SO₄) = 98 г.
N(H₂SO₄) - ?
n(H₂SO₄) - ?
n(H₂SO₄) =
M(H₂SO₄) = Ar(H) * 2 + Ar(S) + Ar(O) * 4 = 1 * 2 + 32 + 16 * 2 = 2 + 32 + 32 =
68 г/моль
n(H₂SO₄) = 98 г. / 68 г/моль ≈ 1,5 моль
N(H₂SO₄) = n * N = 1.5 моль * 6,02 * 10²³ моль⁻¹ = 9,03 частиц
Объяснение:
2 NH4CI+ CaCI2 →t→ 2 NH3↑+ 2H2O
В результате диссоциации образуется гидроксид- анионы(ОН⁻). Аммиак проявляет щелочные свойства.
NH4ОН <==> NH4⁺ +ОН⁻
В лабораторных условиях NH3 получают нагреванием смеси соли аммония и гидроксида.
NH3+HCI→ NH4CI
NH3+HNO3→ NH4NO3
2NH3+ H2SO4→ (NH4)2SO4
Во всех трех пробирках появляется густой белый дым, это говорит об образовании солей аммония. Пары аммиака и кислот образуют пары солей аммония.
При взаимодействии аммиака с кислотами образуются соли аммония.
Дано:
n(Zn) = 0,2 моль
Найти:
m(Zn) - ?
n =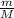 ⇒ m = n * M
⇒ m = n * M
M(Zn) = Ar(Zn) = 65 г/моль
m(Zn) = 0,2 моль * 65 г/моль = 13 г.
ответ: m(Zn) = 13 г.2)Дано:
N(MgO) = 3 * 10²³ частиц
Найти:
m(MgO) - ?
n(MgO) - ?
n(MgO) = =
=  ≈ 0,5 моль
≈ 0,5 моль
m(MgO) = n * M
M(MgO) = Ar(Mg) + Ar(O) = 24 * 16 = 40 г/моль
m(MgO) = 0,5 моль * 40 г/моль = 20 г.
ответ: n(MgO) ≈ 0,5 моль, m(MgO) = 20 г.3)Дано:
m(CO₂) = 22 г.
Найти:
n(CO₂) - ?
N(CO₂) - ?
n(CO₂) =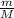
M(CO₂) = Ar(C) + Ar(O) * 2 = 12 + 16 * 2 = 12 + 32 = 44 г/моль
n(CO₂) = 22 г. / 44 г/моль = 0,5 моль
N(CO₂) = n * N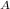 = 0,5 моль * 6,02 * 10²³ моль⁻¹ = 3,01 * 10²³ частиц
= 0,5 моль * 6,02 * 10²³ моль⁻¹ = 3,01 * 10²³ частиц
ответ: n(CO₂) = 0,5 моль, N(CO₂) = 3,01 * 10²³ частиц.4)Дано:
N(Br₂) = 12 * 10²³ частиц
Найти:
m(Br₂) - ?
n(Br₂) - ?
n(Br₂) = =
= 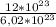 ≈ 2 моль
≈ 2 моль
m(Br₂) = n * M
M(Br₂) = Ar(Br) * 2 = 80 * 2 = 160 г/моль
m(Br₂) = 2 * 160 = 320 г.
ответ: n(Br₂) = 2 моль, m(Br₂) = 320 г.5)Дано:
m(H₂SO₄) = 98 г.
Найти:
N(H₂SO₄) - ?
n(H₂SO₄) - ?
n(H₂SO₄) =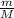
M(H₂SO₄) = Ar(H) * 2 + Ar(S) + Ar(O) * 4 = 1 * 2 + 32 + 16 * 2 = 2 + 32 + 32 =
68 г/моль
n(H₂SO₄) = 98 г. / 68 г/моль ≈ 1,5 моль
N(H₂SO₄) = n * N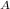 = 1.5 моль * 6,02 * 10²³ моль⁻¹ = 9,03 частиц
= 1.5 моль * 6,02 * 10²³ моль⁻¹ = 9,03 частиц
ответ: n(H₂SO₄) ≈ 1,5 моль, N = 9,03 частицОбъяснение:
2 NH4CI+ CaCI2 →t→ 2 NH3↑+ 2H2O
В результате диссоциации образуется гидроксид- анионы(ОН⁻). Аммиак проявляет щелочные свойства.
NH4ОН <==> NH4⁺ +ОН⁻
В лабораторных условиях NH3 получают нагреванием смеси соли аммония и гидроксида.
NH3+HCI→ NH4CI
NH3+HNO3→ NH4NO3
2NH3+ H2SO4→ (NH4)2SO4
Во всех трех пробирках появляется густой белый дым, это говорит об образовании солей аммония. Пары аммиака и кислот образуют пары солей аммония.
При взаимодействии аммиака с кислотами образуются соли аммония.